Condylomes acuminés : prise en charge et options thérapeutiques
Le condylome acuminé résulte d’une infection par HPV essentiellement par contact direct lors des rapports sexuels. Parmi plus de 100 types de HPV identifiés, 40 souches affectent la région ano-génitale. Les souches HPV 6 et 11 sont parmi les souches les plus répandues impliquées dans le développement des condylomes acuminés (plus rarement 30, 42, 43). La prévalence de cette infection HPV augmente depuis les années 70 et affecterait 6 à 10 % de la population générale : 2 fois plus que celle de l’herpès génital. Leur apparition coïncide avec l’âge des premiers rapports sexuels. Les préservatifs ne protègent pas à 100 % contre l’infection.
Le poids des infections HPV : une morbidité mondiale tous azimuts
Plusieurs souches de HPV sont susceptibles de provoquer une dysplasie cellulaire conduisant à certains cancers, à savoir celui du col de l’utérus chez la femme et le cancer du pénis ou du rectum chez l’homme4. Les types HPV 16 et 18 sont des sous-types à haut risque de développer une tumeur maligne. La recherche a solidement établi leur rôle dans le développement des carcinomes cervicaux, ano- génitaux et buccaux. Les types de HPV 31, 33, 35, 39, 45, 51, 52, 56, 58, 59, 66, 68, 73 et 82 peuvent également être oncogènes. Les cancers cutanés autres que le mélanome sont corrélés aux types de HPV 1, 5, 8, 9, 17, 20, 23 et 38. La maladie de Bowen a des corrélations avec les types 16, 18, 31, 32 et 34 du HPV. L’épidermodysplasieverruciforme a été associée aux HPV de types 5, 8, 9, 12, 14, 15, 17, 19-25, 36-38, 46, 47, 49 et 50. Les types de HPV 6 et 11 présentent un faible risque de développer une tumeur maligne et provoquent 90% des verrues ano-génitales. Quant aux verrues cutanées elles sont associées aux types de HPV 1, 2, 3, 4, 27 et 57.5
Les facteurs de risques de
contamination des HPV sont connus
L’infection HPV est l’infection sexuellement transmissible la plus répandue dans le monde avec 9 à 13% de la population mondiale infectée.4 Les patients âgés de 20 à 39 ans sont les plus fréquemment touchés.6 Il existe plusieurs facteurs de risque de contamination par un virus HPV.
La prévalence de l’infection augmente avec :
• Le nombre de partenaires sexuels
• Les antécédents d’infections à chlamydia et gonorrhée
• Le tabagisme
• L’infection par le virus de l’immunodéficience humaine (VIH).4, 7
• La sodomie est vraisemblablement un facteur de risque majeur
• Les caresses intimes (sans pénétration) suffisent à assurer la transmission du virus10.
Tout patient présentant des condylomes doit bénéficier d’un dépistage d’autres IST parfois asymptomatiques : VIH, syphilis, hépatite, chlamydia trachomatis, herpès simplex virus (HSV) type 2 ou VIH. Ces infections favoriseraient l’apparition de lésions précancéreuses et prédisposeraient au cancer en affaiblissant les défenses immunitaires de l’hôte.
Autres facteurs de risque :
• La fumée produite lors de la destruction des condylomes au bistouri électrique ou au laser.
• La contamination laryngée du nouveau-né lors de l’accouchement.
• Plus exceptionnellement : sextoys et spéculum, anuscopes, pinces à biopsie mal sterilisés.
• Les situations de déficit immunitaire
Condylomes acuminés : physiopathologie
Les HPV sont des virus à ADN double brin qui infectent principalement le noyau des cellules épithéliales squameuses différenciées. Ils peuvent rester quiescents pendant plusieurs mois : la période d’incubation est d’un mois à deux ans9.
Le génome des HPV contient un oncogène qui code des protéines qui stimulent la prolifération cellulaire. Ces protéines permettent aux virus de se répliquer via l’ADN polymérase de la cellule hôte tandis qu’elles se divisent. Au fur et à mesure que le nombre de cellules hôtes infectées par le virus augmente, les couches basales, épineuses et granulaires de l’épiderme s’épaississent, entraînant une acanthose et l’apparition macroscopique de verrues. Le condylome acuminé prend généralement trois à quatre mois pour se développer. Chez des individus par ailleurs en bonne santé, une réponse immunitaire adéquate est susceptible d’arrêter la réplication virale et résoudre l’infection au fi l du temps. Cependant, une infection prolongée au HPV augmente le risque de développer une transformation maligne10. Le condylome acuminé est généralement un diagnostic clinique et l’examen histopathologique des lésions n’est généralement pas nécessaire. Une évaluation microscopique du tissu montrera une acanthose avec une hyperkératose susjacente. Le condylome acuminé se différencie de la verruca vulgaris : une hyperplasie verruqueuse à pointes est observée dans la verrue vulgaire, tandis que la papillomatose se manifeste dans le condylome acuminé.11
La clinique
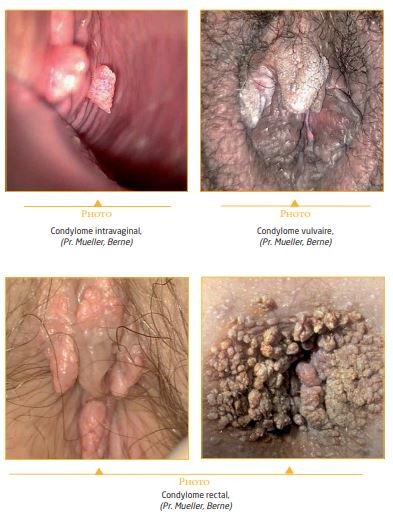
Le diagnostic essentiellement clinique doit être visuellement fait à bon éclairage et ne pas hésiter à utiliser une loupe en cas de doute : on visualisera en général au sommet des condylome de petites ponctuations vasculaires caractéristiques. Les condylomes sont en général localisés12 sur le vestibule, les petites et grandes lèvres voire même en intra vaginal. La région anale peut aussi être atteinte dans environ 20% des cas si atteinte vulvaire. Certaines lésions peuvent exister sur la marge et le canal anal, le col utérin, voire également être présentes dans la cavité buccale, sur la langue et la lèvre 11, sur le pubis, … En cas de découverte de lésions de la marge anale, l’anuscopie doit être systématique dans les 2 sexes. L’atteinte du col impose un frottis avant 30 ans et un test HPV après 30 ans.
Chez l’homme les lésions sont habituellement localisées au sillon balano- préputial, ou au fourreau de la verge et fréquemment à la région péri-anale chez l’homosexuel. Ne pas oublier ici de rechercher une atteinte urétrale du premier cm (plus rare chez la femme) : la localisation au méat ou à l’urètre est présente dans 20 à 25 % des cas et l’urétroscopie est alors nécessaire pour les lésions dont le pôle supérieur des lésions ne peut être visualisé par l’éversion des berges du méat.
Le nombre de patients consultant annuellement en France serait de 130 000. Le coût global annuel direct à environ 54 millions d’euros, dont 36 millions d’euros à la charge de l’Assurance Maladie. Les infections latentes méconnues sont beaucoup plus fréquentes que les formes visibles, surtout chez la femme. Lorsque le condylome est visible, les patients se présentent généralement préoccupés par l’apparence des lésions provoquant souvent détresse psychologique et angoisse. Les condylomes acuminés peuvent également être retrouvés fortuitement chez la femme lors d’examens gynécologiques de routine. L’apparence de la lésion dépend du type de HPV et du site d’infection.10
Recommandations thérapeutiques de la Société Française de Dermatologie20
1) lésions limitées en nombre et en taille
• cryothérapie
• ou imiquimod
• ou podophyllotoxine (sauf vulve et anus)
2) lésions nombreuses (> 10) ou étendues (> 1 cm2)
1er épisode :
· Imiquimod
· Ou destruction (laser, chirurgie, électrocoagulation)
Récidives : Destruction (laser, chirurgie, électrocoagulation)
• Les condylomes acuminés, ou végétations vénériennes, exophytiques, blanchâtres, (« crêtes de coq ») sont les plus fréquentes et se présentent généralement sous la forme de papules charnues en relief, de couleur peau et dont la taille varie de 1à 5 millimètres de diamètre. Ils peuvent être larges et plats, pédonculés ou parfois avoir une apparence de chou-fleur.10
• Les lésions papuleuses, pigmentées ou non (certaines lésions sont rouges ou leucoplasiques à biopsier car elles présentent un éventuel potentiel oncogène)
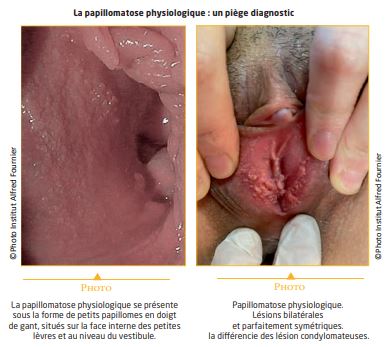
• Les condylomes plans sont des lésions à peine visibles à visualiser sous formes de macules blanches après application d’acide acétique à 5 %.
Si une masse tumorale importante occupe toute la zone ano-génitale, les tumeurs de BuschkeLöwenstein, complication maligne du condylome acuminé13, doivent être évoquées. Des tests supplémentaires sont parfois nécessaires pour faire le diagnostic. Le colposcope peut être utile pour agrandir les lésions pour une meilleure visualisation. Les tests de confirmation et le typage génique sont possibles via des tests de détection d’ADN tels que la réaction en chaîne par polymérase (PCR). Enfin, le test à l’acide acétique peut être utilisé pour évaluer davantage la lésion. En cas de suspicion de dysplasie une biopsie de la lésion est indiquée2. Chez les enfants atteints de condylomes acuminés un possible abus sexuel doit être suspecté.
Les traitements
Le traitement vise à faire disparaître les lésions visibles. Il est basé sur la simple destruction locale au bistouri électrique, au laser, à l’azote liquide et/ou à l’aide d’un traitement topique. La difficulté principale réside dans le caractère souvent multifocal des lésions et leur taux élevé de récidives dont il faut informer le patient. Parmi les options de traitements :
• La cryothérapie : c’est le traitement de choix, souvent de première intention pour les lésions de petite taille. L’azote liquide est appliqué avec un coton-tige ou un pulvérisateur (CRYAC). L’efficacité est de 63% à 89%.
• Le laser nécessite une anesthésie locale, voire générale en fonction de l’étendue des lésions. L’efficacité se situe entre 80% à 90%.
• L‘électrocoagulation au bistouri électrique se pratique au bloc opératoire sous anesthésie générale avec des résultats équivalents à ceux rapportés pour le laser et sont de 80% à 93%.
• L’imiquimod crème 5% (Aldara®) est un traitement immunomodulateur qui s’applique en fines couches trois fois par semaine le soir. La région exposée doit être soigneusement rincée le matin. La durée du traitement ne doit pas dépasser 16 semaines. On observe souvent un érythème avec des sensations de brûlures, parfois des ulcérations. Ce traitement montre une efficacité de 45% à 67%. La crème Aldara® doit être administrée avec prudence chez les femmes enceintes.
• La podophyllotoxine (Condyline 0,5 %®), préparée à partir d’extraits de plantes et appliquée matin et soir pendant 3 jours consécutifs, chaque semaine pendant un maximum de 5 semaines successives. La disparition des lésions à 60-80% après application de podophyllotoxine en crème 0,15% a été décrite3, 4. La Condyline® est contre-indiquée chez les femmes enceintes.
• Le 5-Fluoro-uracile (5-FU) en crème (Efudix® 5%) est appliqué en couches fines 1 à 3 fois par semaine pendant 6 semaines. Cette crème doit être réservée à une application vulvaire avec une efficacité de 60% à 90% en évitant les lésions de la marge anale. Efudix® est contre-indiqué chez les femmes enceintes.
• La pommade à 10% de sinécatéchines (Veregen 10%) utilisée trois fois par jour jusqu’à seize semaines
si nécessaire. Il s’agit d’extraits de thé vert, crème à appliquer en couche fine. Ce produit n’a pas eu l’agrément en France pour SMR insuffisant.
• L’acide trichloracétique (TCA) 80 à 90% est un traitement disponible pour les petites lésions. Après l’application, un petit ulcère se forme et guérit sans laisser de cicatrices. Le TCA est appliqué une fois par semaine pendant huit à dix semaines.
• Enfin, une exérèse chirurgicale peut être réalisée pour les lésions réfractaires au traitement ou très étendues. Les options chirurgicales comprennent, le bistouri électrique, l’excision et la thérapie au laser.
Bien que le condylome acuminé puisse être difficile à traiter, la maladie est guérissable. Cependant, les lésions peuvent nécessiter plusieurs traitements ou une combinaison de traitements au fil du temps. L’excision chirurgicale est la seule option de traitement avec des taux de clairance proches de 100%, bien que le condylome acuminé puisse réapparaître après tous les types de traitement.
L’évolution des condylomes se fait par l’augmentation du nombre et de la taille des lésions. Le risque majeur des condylomes acuminés est d’évoluer vers le carcinome épidermoïde, ce qui justifie leur traitement énergique. Ainsi le potentiel oncogène des condylomes est entre autres responsable de l’augmentation de l’incidence des cancers de l’anus. Les signes de transformation maligne comprennent des saignements, une pigmentation irrégulière, une ulcération et des lésions avec infiltration cutanée palpable. 14 Les tumeurs de Buschke-Löwenstein sont une complication connue du condylome acuminé.13
En conclusion
Il est impératif d’informer les parents des avantages des vaccins contre les HPV dont l’efficacité est très importante15.
Le vaccin quadrivalent protège contre HPV 6 et 11, responsables d’environ 90% des verrues génitales et contre HPV 16 et 18, responsables de 70 à 80% des cancers du col de l’utérus 16. Le vaccin nonavalent actuellement disponible protège, outres les HPV 6 et 11 contre HPV 16 et 18 + 5 autre souches de HPV oncogènes (31, 33, 45, 52, 58). Les recommandations actuelles sont de vacciner les filles et les garçons âgés de préférence entre 11 à 14 ans17,18. La vaccination des garçons est désormais remboursée en France à compter du 1 er janvier 2021.
Les auteurs déclarent ne pas avoir de liens d’intérêt avec cet article
René Druckmann, Nice
David Elia, Paris
RÉFÉRENCES
1 – O’Mahony C, Gomberg M, Skerlev M, Alraddadi A, de Las Heras-Alonso ME, Majewski S, Nicolaidou E, Serdaroğlu S, Kutlubay Z, Tawara M, Stary A, Al Hammadi A, Cusini M. Position statement for the diagnosis and management of anogenital warts. J Eur Acad Dermatol Venereol. 2019 juin; 33 (6): 1006-1019
2 – Aubin F,Prétet JL,Jacquard AC,Saunier M,Carcopino X,Jaroud F,Pradat P,Soubeyrand B,Leocmach Y,Mougin C,Riethmuller D;EDITH Study Group. Human papilloma iris genotype distribution in external acuminata condylomata: a Large French National Study (EDITH IV) , Clin Infect Dis 2008 Sep 1;47(5);610-5 F,
3 – Maw R., HPV Special Intrest Goup of BASHH.Anogenital warts. Sex Transm Infect. 2006 Dec; 82 Suppl 4: iv40-1.
4 – Kaderli R, Schnüriger B, Brügger LE. The impact of smoking on HPV infection and the development of anogenital warts. Int J Colorectal Dis. 2014 août ; 29 (8) : 899-908.
5 – Brianti P, De Flammineis E, Mercuri SR. Review of HPV-related diseases and cancers. Nouveau Microbiol. 2017 Avr; 40 (2): 80-85.
6 – Fleischer AB, Parrish CA, Glenn R, Feldman SR. Condylomata acuminata (genital warts) patient demographics and treating physicians. Sex Transm Dis. 2001 novembre; 28 (11): 643-7.
7 – Chelimo C, Wouldes TA, Cameron LD, Elwood JM. Risk factors for and prevention of human papillomaviruses (HPV), genital warts and cervical cancer. J Infect. 2013 Mar;66(3):207-17.
8 – Park IU, Introcaso C, Dunne EF. Human Papillomavirus and Genital Warts: A Review of the Evidence for the 2015 Centers for Disease Control and Prevention Sexually Transmitted Diseases Treatment Guidelines. Clin Infect Dis. 2015 Dec 15;61 Suppl 8 : S849-55.
9 – Varma S, Lathrop E, Haddad LB. Pediatric condyloma acuminata. J Pediatr Adolesc Gynecol. 2013 Dec;26(6):e121-2.
10.Costa-Silva M, Fernandes I, Rodrigues AG, Lisboa C. Anogenital warts in pediatric population. An Bras Dermatol. 2017 Sep-Oct;92(5):675-681.
11 – Betz SJ. HPV-Related Papillary Lesions of the Oral Mucosa: A Review. Head Neck Pathol. 2019 Mar;13(1):80-90.
12 – Sykes NL. Condyloma acuminatum. Int J Dermatol. 1995 May;34(5):297-302.
13 – Sporkert M ,Rübben A.( Buschke-Löwenstein tumors). Hautarzt 2017 Ma;68(3):199-203
14 – Lacey CJ,Woodhall SC,Wikstrom A,Ross J.2012 European guidelines for the management of anogenital warts.J Eur Acad Dermatol Venerol.2013 Mar;27(3):e263-70
15 – Scheinfeld N.Update on the treatment of genital warts Dermatol Online J.2013 Jun 15;19(6):18559
16 – Castle PE,Maza M.Prophylactic HPV vaccination:past,present and future.Epidemiol Infect.2016 Feb;144(3):449-68
17 – Baechler Dc,Gonzales FA,Kobrin SC,Kreimer AR.HPV vaccination initiation after the routine-recommended ages of 12-12 in the United States. Papillomavirus Res.2016 Dec 01;2:11-16
18 – https://www.has-sante.fr/jcms/p_3116022/fr/recommandation-sur-l-elargissement-de-la-vaccination-contre-les-papillomavirus-aux-garcons
19 – Moscicki AB, Schiffman M, Burchell A, Albero G, Giuliano A, Goodman MT, Kjaer SK, Palefsky J. Updating the natural history of human papillomavirus and anogenital cancers. Vaccine 2012;30 (Suppl. 5):F24-F33
20 – Recommandations thérapeutiques de la Société Française de Dermatologie








46 commentaires